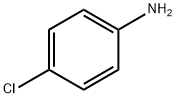
| Opis |
p-Hloroanilin, 1-amino-4- hlorobenzen, je bijela do svijetlo žuta, kristalna čvrsta supstanca na sobnoj temperaturi. Koristi se kao međuprodukt za pesticide, farmaceutske proizvode, pigmente i boje. Proizvodnja je slična onoj kod m-kloroanilina. |
| Hemijska svojstva |
4-Hloroanilin je bezbojna do blago jantarna kristalna čvrsta supstanca s blagim aromatičnim mirisom. Rastvorljiv je u vrućoj vodi i organskim rastvaračima. 4-Hloroanilin ima umjeren pritisak pare i koeficijent raspodjele n-oktanol/voda. Razlaže se u prisustvu svetlosti i vazduha i na povišenim temperaturama. |
| Fizička svojstva |
Žućkasto-bela čvrsta supstanca sa blagim, slatkastim mirisom. Prag koncentracije mirisa je 287 ppm (citirano, Keith i Walters, 1992). |
| Koristi |
4-Kloroanilin je važna sirovina u proizvodnji poljoprivrednih hemikalija, azo boja i pigmenata, kozmetike i farmaceutskih proizvoda. Koristi se kao intermedijer u proizvodnji hromofora AS-LB, kao i u farmaceutskim intermedijerima kao što su hlordiazepoksid i tinktura fena. Također je međuprodukt za herbicid Anilofos, insekticid hlorbenzuron i regulator rasta biljaka Inabenfide. |
| Definicija |
ChEBI: 4-hloroanilin je hloroanilin u kojem je hloro atom para u odnosu na anilin amino grupu. To je hloroanilin i član monoklorobenzena. |
| Aplikacija |
4-Hloroanilin je važan građevinski element koji se koristi u hemijskoj industriji za proizvodnju lijekova i bojila. Neki benzodiazepinski lijekovi koriste 4-hloroanilin u svojoj proizvodnji. |
| Priprema |
sinteza 4-hloroanilina: p-hloronitrobenzen se koristi kao sirovina, Raney nikal se koristi kao katalizator, etanol se koristi kao rastvarač, temperatura reakcije je 50-70 stepen, pritisak hidrogenacije je 3.{{4} }.55MPa i srednji pH=5-6 uslovi, izvedite reakciju katalitičke hidrogenacije da biste dobili 4-hloroanilin. |
| Reference za sintezu |
Journal of the American Chemical Society, 99, str. 98, 1977DOI:10.1021/ja00443a018
Sinteza, str. 48, 1987DOI: 10.1055/s-1987-27838 |
| Opći opis |
P-kloroanilin se pojavljuje kao bijela ili blijedožuta čvrsta supstanca. Tačka topljenja 69,5 stepeni. |
| Reakcije zraka i vode |
Nerastvorljivo u hladnoj vodi. Rastvorljivo u vrućoj vodi [Hawley]. |
| Profil reaktivnosti |
4-Hloroanilin je nekompatibilan sa oksidantima. Takođe nekompatibilan sa kiselinama, kiselim hloridima, anhidridima kiselina i hloroformatima. Podložan egzotermnoj razgradnji tokom visokotemperaturne destilacije. Nekompatibilno sa azotnom kiselinom. |
| Hazard |
Toksično ako se udiše i guta. Mogući kancerogen. |
| Opasnost po zdravlje |
Udisanje ili gutanje izaziva plavkastu nijansu noktiju, usana i ušiju što ukazuje na cijanozu; glavobolja, pospanost i mučnina, praćeni gubitkom svijesti. Tečnost se može apsorbirati kroz kožu i uzrokovati slične simptome. Kontakt sa očima izaziva iritaciju. |
| Opasnost od požara |
Posebne opasnosti od proizvoda sagorevanja: Iritirajući i otrovni hlorovodonik i oksidi azota mogu se stvoriti u požaru. |
| Zapaljivost i eksplozivnost |
Zapaljivo |
| Sigurnosni profil |
Potvrđen kancerogen s eksperimentalnim neoplastigenim i tumorigenim podacima. Otrov gutanjem, udisanjem, sh kontaktom, subkutanim i intravenskim putem. Jako nadražuje kožu i oči. Podaci o mutaciji prijavljeni. Kada se zagrije do raspadanja, emituje otrovne pare Cland NOx. Vidi također ANILINSKE BOJE |
| Sudbina životne sredine |
Biološki.U anaerobnom mediju, bakterije Paracoccus sp. pretvorio 4- hloroanilin u 1,3-bis(p-hlorofenil)triazen i 4-hloroacetanilid sa prinosom proizvoda od 80 i 5%, respektivno (Minard et al., 1977). U terenskom eksperimentu, [14C]4-hloroanilin je primijenjen na tlo na dubini od 10 cm. Nakon 20 tjedana, 32,4% primijenjene količine je prikupljeno u tlu. Identifikovani metaboliti uključuju 4-hloroformanilid, 4-hloroacetanilid, 4-hloronitrobenzen, 4- hloronitrozobenzen, 4,4′-dihloroazoksibenzen i 4,4′-dihloroazobenzen (Freitag et al. , 1984).
Zemlja.4-Hloroanilin se kovalentno vezuje sa humatima u tlu kako bi formirao kvinoidne strukture nakon čega slijedi oksidacija da bi se dobio hinoidni prsten supstituiran dušikom. Poluživot reakcije od 13 minuta je određen sa jednim huminskim spojem (Parris, 1980). Katehol, monomer huminske kiseline, reagovao je sa 4-kloroanilinom dajući 4,5-bis(4-klorofenilamino)-3,5-cikloheksadien-1, 2-dione (Adrian et al., 1989).
Fotolitički.Under artificial sunlight, river water containing 2–5 ppm 4-chloroaniline photodegraded to 4-aminophenol and unidentified polymers (Mansour et al., 1989). Photooxidation of 4-chloroaniline (100 μM) in air-saturated water using UV light (λ >290 nm) produced 4-chloronitrobenzene and 4-chloronitrosobenzene. About 6 h later, 4-chloroaniline completely reacted leaving dark purple condensation products (Miller and Crosby, 1983). In a similar study, irradiation of an aqueous solution in the range of 290–350 nm resulted in the formation of the intermediate 4-iminocyclohexa-2,5-dienylidene (Othmen et al., 2000). A carbon dioxide yield of 27.7% was achieved when 4-chloroaniline adsorbed on silica gel was irradiated with light (λ >290 nm) tokom 17 h (Freitag et al., 1985).
Konstanta brzine 8,3 x 10-11cm3/molecule?sec je prijavljen za reakciju u gasnoj fazi 4- hloroanilina i OH radikala u vazduhu (Wahner i Zetzsch, 1983).
Hemijska/fizička.4-Hloroanilin neće hidrolizirati u razumnoj mjeri (Kollig, 1993).
Pizzigallo et al. (1998) istraživali su reakciju 4-hloroanilina sa željeznim oksidom i dva oblika mangan dioksida [birnesit (δ-MnO2) i piroluzit (MnO2)] u pH opsegu od 4-8 na 25 stepeni. Brzina reakcije 4-hloroanilina bila je redom birnesit > piroluzit > željezni oksid. Na pH 4.{10}}, reakcija s birnessitom bila je toliko brza da se reakcija nije mogla odrediti. Poluživot za reakciju 4-hloroanilina sa piroluzitom i željeznim oksidom bio je 383 i 746 minuta, respektivno. Brzina reakcije se smanjivala kako se pH povećavao. Jedina oksidaciona jedinjenja identifikovana GC/MS su 4,4′-dihloroazobenzen i 4-hloro-4′-hidroksidifenilamin. |
| Metode prečišćavanja |
Kristalizirajte anilin iz MeOH, pet etera (b 30-60o) ili 50% vodenog EtOH, zatim *benzen/pet etera (b 60-70o), a zatim ga osušite u vakuumskom eksikatoru. Može se destilovati pod vakuumom (b 75-77o/3mm). Sublimira se u veoma visokom vakuumu. Acetat kristalizira iz vodenog MeOH (m 178o, 180o) ili EtOH ili AcOH (m 173-174o) i ima b 331,3o/760 mm. [Beilstein 12 III 1325, 12 IV 1116.] |