| Outline |
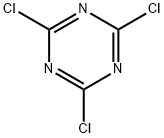
Cijanurični hlorid, bijeli kristali sa jakim iritirajućim mirisom hlora, korozivan je za kožu, ima iritaciju očiju i suzenje. Tačka topljenja 145 stepeni, tačka ključanja 190 stepeni, UVλmax241nm (etanol). Rastvorljiv je u etanolu, etil etru, hloroformu, sirćetnoj kiselini i akrilonitrilu, nerastvorljiv u hladnoj vodi. hlađenje reakcije cijanuric hlorida i vode je sporo, kada se zagrije brzo se hidrolizira u cijanuricnu kiselinu (C3H3O3N3) i hlorovodoničnu kiselinu, produkti su relativno rastvorljivi u vodi, tako da možete koristiti metod ekstrakcije odvajanja. Reagira s koncentriranom dušičnom kiselinom i koncentriranom sumpornom kiselinom na sobnoj temperaturi kako bi se djelomično pretvorila cijanurska kiselina, a reagira s natrijum alkoksidom kako bi se stvorio triester cijanurske kiseline, a također može reagirati s amonijakom, aminima, fenolima i tako dalje.
Posljednjih godina u Kini postoji brzi rast potrošnje cijanuric hlorida, od 1998. do 2004 prosječna godišnja stopa rasta prividne potrošnje bila je oko 32,2% , 2005. potražnja za cijanuric hloridom dostigla je 50,{{ 6}} tona, prema prognozama, od 2007. do 2012. cijanuric hlorid će nastaviti brzi rast prosječnom stopom od 6,0%, tržište je vrlo obećavajuće. Budući da su naknadni proizvodi cijanuric hlorida enormni, potražnja na tržištu je velika, nacionalne istraživačke institucije i srodna preduzeća su nastavili da razvijaju svoje dalje proizvode i otvaraju aplikacije za cijanuric hlorid. Zbog toga se pojavljuju novi proizvodi derivata cijanuric hlorida, a potražnja na tržištu će se dalje širiti.
Povezane hemijske reakcije cijanuric hlorida koje uključuju:
Nakon 2-amino-4-nitrofenolne diazotizacije i spajanja H kiselina, te naknadne obrade kompleksa hroma i kobalta, prvo se kondenzira sa cijanuric hloridom, a zatim nakon kondenzacije sa amonijakom da se dobije reaktivni crni K-BR. Uglavnom se koristi za štampanje pamuka, poliestera/pamuka.
Sa cijanuric hloridom kao sirovinom, u rastvoru trihloretilena na 20~30 stepeni, sa reakcijom amina, 2,4-dihloro-6-etil-1,3,5-triazin je proizveden, a zatim reaguje sa amonijakom da bi proizveo 2-amino-4-hloro-6-etilamino triazin, a zatim reaguje sa 2-hloro-2-metil propionitrilom, koji može proizvesti selektivne herbicide cijanazin za kontrolu jednogodišnjih ili višegodišnjih uskih listova ili širokolisnih korova u polju kukuruza. |
| Hemijska svojstva |
Kristali koji imaju oštar miris. Rastvorljiv u hloroformu, tetrahloridu ugljenika, etanolu, vrućem eteru, acetonu, dioksanu, slabo rastvorljiv u vodi. |
| Koristi |
cijanuric hlorid je važan fini hemijski proizvod, sa širokim spektrom upotrebe, intermedijer je u industriji pesticida i proizvodnji sirovine za reaktivne boje, može se koristiti kao sve vrste organskih aditiva za industrijsku proizvodnju, kao što su fluorescentni izbeljivači, tekstilne tvari otporne na skupljanje, površinski aktivna sredstva, jedan je od materijala koji se koristi u proizvodnji odbrambenih eksploziva i gumenih ubrzivača, a također je i materijal za sintezu lijekova u pesticidnoj i farmaceutskoj industriji.
Gore navedene informacije uređuju Chemicalbook Tian Ye. |
| način proizvodnje |
Proces proizvodnje cijanuric hlorida obično se sastoji od dva koraka: polimerizacija hlorid cijanogena i priprema hlorid cijanogena. Postoji mnogo načina za stvaranje hlorid cijanogena, kao što je sinteza metil tiocijanata i hlora, cijanovodonična kiselina se otapa u hloroformu i gas hlor se stavlja u sintezu, metoda cijanovodične kiseline, natrijum cijanid, urea, cijanovodična kiselina direktna metoda hlora i cijanuric klorid i slično, trenutna proizvodnja industrijskog cijanuric klorida općenito koristi natrijum cijanid i cijanovodičnu kiselinu kao sirovine na dva načina. 1. Metoda natrijum cijanida: koristeći natrijum cijanid kao sirovinu nakon reakcije hlora i cijanuric hlorida, polimerizuje se da bi se formirao cijanuric hlorid, gasi se, a zatim se nakon kristalizacije dobija proizvod. Potrošnja materijala fiksna: natrijum cijanid 1073kg/t, hlor 1700kg/t. 2. Metoda cijanovodične kiseline: sa cijanovodoničnom kiselinom kao sirovinom, hlorid cijanogen se proizvodi reakcijom hlora, a zatim se koristi polimerizacija za stvaranje cijanuric hlorida, gašenje, kristalizacija, dobija se proizvod. Potrošnja materijala fiksna: cijanovodonična kiselina 500kg/t, hlor 1200kg/t. |
| Kategorija |
korozivne supstance |
| Ocjenjivanje toksičnosti |
Srednje toksičan |
| Akutna toksičnost |
Oralni LD50 pacova: 485 mg/kg; Oralno-miš LD50: 350 mg/kg |
| Podaci o iritaciji |
koža-zeč 500 mg/24 sata umjereno; Oči-zec 0,05 mg/24 sata teške |
| Zapaljivost i karakteristike opasnosti |
Kada je u kontaktu sa vodom, emituje otrovni gas hlorovodonik; kada je termički razgrađuje otrovni gas hlorovodonika |
| Karakteristike skladištenja |
Ventilirano, niskotemperaturno, suvo skladište. Čuva se odvojeno od oksidanata i lužina. |
| Sredstvo za gašenje |
ugljen dioksid, suvi prah, peskovito tlo |
| Hemijska svojstva |
Bijeli prah |
| Koristi |
Cijanurhlorid je međuprodukt za proizvodnju agrohemikalija (triazinski herbicidi), bojila, optičkih izbjeljivača, sredstava za štavljenje, reaktivnih boja, agenasa koji apsorbiraju UV zrake, sredstava za omekšavanje i farmaceutskih proizvoda, kao i blok-buildera za plastiku. List sa podacima o proizvodu |
| Koristi |
Cijanuhlorid je međuprodukt za proizvodnju agrohemikalija, bojila, optičkih izbjeljivača, sredstava za štavljenje, sredstava za omekšavanje i farmaceutskih proizvoda, kao i za izradu blokova za plastiku. |
| Koristi |
Reagens za pretvaranje alkohola u kloride i za imobilizaciju mikroorganizama i enzima.1 |
| Koristi |
Cijanuric hlorid se intenzivno koristi u pripremi pesticida i herbicida klase triazina. Cijanuric hlorid se također koristi kao prekursor boja i agenasa za umrežavanje zbog reaktivnih atoma hlora prema reakcijama nukleofilne supstitucije. Derivati cijanuric hlorida imaju širok spektar delovanja kao antibakterijskih i antikancerogenih agenasa. |
| Koristi |
Intermedijer u sintezi aktivnih boja, poljoprivrednih proizvoda i ljekovitih tvari. Reagens u organskoj sintezi. Sredstvo za spajanje nukleinskih kiselina i proteina; Papir aktiviran cijanuričnim hloridom koristi se u kapilarnim i elektrobloting aplikacijama, dot testovima i hibridizacijskim protokolima. |
| Definicija |
ChEBI: hloro-1,3,5-triazin u kojem je triazinski prsten na svakom ugljeniku zamijenjen hlorom. Njegova glavna upotreba je u pripremi pesticida klase triazina. |
| Metode proizvodnje |
Cijanuric hlorid se dobija trimerizacijom cijanogen hlorida u organskim rastvaračima, u prisustvu kiselih katalizatora, i izvodi se u gasovitoj fazi na 200–500 C. Cijanuric hlorid se koristi kao hemijski intermedijer. To je prekursor herbicida atrazina. |
| Opći opis |
Bezbojna kristalna čvrsta supstanca oštrog mirisa. Tačka topljenja 146 stepeni. Gustina 1,32 g/cm3. Vrlo slabo rastvorljiv u vodi. Toksično gutanjem i udisanjem para. Iritira kožu i oči. Koristi se za pravljenje boja. |
| Reakcije zraka i vode |
Reaguje egzotermno s vodom, posebno ako je katalizirana ili zagrijana, stvarajući pare hlorovodonične kiseline. Vrlo slabo rastvorljiv u vodi. |
| Profil reaktivnosti |
Cijanuric hlorid reaguje brzo i egzotermno sa vodom i stvara hlorovodonik. Mješavina s vodom u industrijskom reaktoru s isključenim hlađenjem razvila je pritisak koji je raznio zaptivke i ispunio zgradu zapaljivim parama. Eksplozija se dogodila kada su pare zapaljene [MCA Case History 1869(1972)]. Došlo je do nepovratnih reakcija sa acetonom/vodom; metanol/voda, etoksietanol/voda, alil alkohol/natrijum hidroksid/voda, 2-butanon/natrijum hidroksid/voda i metanol/natrijum bikarbonat [Loss Prev. Bul., 1979, (25), 21]. Reaguje sa metanolom dajući gasoviti metil hlorid. Brzo reaguje s bikarbonatima i stvara plinoviti ugljični dioksid. Snažno reaguje sa dimetil formamidom (DMF) kako bi se formirao ugljen dioksid nakon obmanjujućeg perioda indukcije [BCISC Quart. Safety Summ., 1960, 35, 24]. Može reagirati s redukcijskim agensima kako bi se stvorila toplina i proizvodi koji mogu biti plinoviti (izazivajući pritisak u zatvorenim posudama). Proizvodi mogu i sami biti sposobni za dalje reakcije (kao što je sagorijevanje na zraku). |
| Opasnost po zdravlje |
TOXIC; udisanje, gutanje ili kontakt (koža, oči) s parama, prašinom ili tvarima može uzrokovati teške ozljede, opekotine ili smrt. Reakcija s vodom ili vlažnim zrakom oslobađa otrovne, korozivne ili zapaljive plinove. Reakcija s vodom može stvoriti mnogo topline koja će povećati koncentraciju isparenja u zraku. Vatra će proizvesti iritirajuće, korozivne i/ili toksične gasove. Otjecanje iz vode za kontrolu požara ili vode za razrjeđivanje može biti korozivno i/ili toksično i uzrokovati zagađenje. |
| Opasnost od požara |
Negoriva, supstanca sama po sebi ne gori, ali se može razgraditi pri zagrijavanju i proizvesti korozivne i/ili toksične pare. Pare se mogu akumulirati u zatvorenim prostorima (podrum, cisterne, rezervoari/cisterne itd.). Supstanca će reagovati sa vodom (neke burno), oslobađajući korozivne i/ili toksične gasove i oticanje. Kontakt sa metalima može razviti zapaljivi vodonik. Kontejneri mogu eksplodirati kada se zagriju ili ako su kontaminirani vodom. |
| Zapaljivost i eksplozivnost |
Nije zapaljivo |
| Sigurnosni profil |
Otrov gutanjem, inhalacijom i intravenskim putem. Upitan kancerogen s eksperimentalnim tumorogenim podacima. Eksperimentalni reproduktivni efekti. Korozivna. Jako nadražuje kožu i oči. Alergen. Prijavljeno je da uzrokuje iritaciju sluzokože i poremećaje srčanog ritma kod ljudi. Burna reakcija sa vodom - (iznad 30 stepeni), aceton + voda, metanol, metanol + natrijum hidrogenkarbonat, 2- etoksietanol, dimetil formamid, 3- butanon + natrijum hidroksid + voda, alil alkohol + natrijum hidroksid + voda (na 28 stepeni). Kada se zagrije do raspadanja, emituje otrovne pare Cland NOx. Vidi također HLORIDI. |
| Metode prečišćavanja |
TCT kristalizira iz CCl4 ili pet etera (b 90-100o) i suši se pod vakuumom. Također je dva puta prekristaliziran iz bezvodnog *benzena neposredno prije upotrebe [Abuchowski et al. J Biol Chem 252 3582 1977]. [Beilstein 26 III/IV 66.] |