
Uvod u proizvod
| Kalcijum fluorid Osnovne informacije |
| Hemijska svojstva kristalna struktura Koristi Metoda proizvodnje |
| Naziv proizvoda: | Kalcijum fluorid |
| Sinonimi: | Kalcijum fluorid; Kalcijum fluorid, 99,9% metala u tragovima; Kalcijum fluorid, 99,95% metala u tragovima; Kalcijum fluorid, bezvodni, ampulisan pod argonom, 99,99% metala u tragovima; Kalcijum fluorid u Kini (CANTI-CN) antitelo; proizveden u zecu;CAF1-poput proteina;CALIFp |
| CAS: | 7789-75-5 |
| MF: | CaF2 |
| MW: | 78.07 |
| EINECS: | 232-188-7 |
| Kategorije proizvoda: | Neorganski; metal halogenid |
| Mol fajl: | 7789-75-5.mol |
 |
|
| Hemijska svojstva kalcijum fluorida |
| Tačka topljenja | 1402 stepena |
| Tačka ključanja | 2500 stepeni (lit.) |
| gustina | 3,18 g/mL na 25 stepeni (lit.) |
| indeks loma | 1.434 |
| Fp | 2500 stepeni |
| temp. | -20 stepen |
| rastvorljivost | Slabo rastvorljiv u kiselini; nerastvorljivo u acetonu. |
| formu | rod |
| boja | bela |
| Specifična težina | 3.18 |
| Rastvorljivost u vodi | 0.015 g. na 100g H20 na sobnoj temperaturi.(NERASTVIV) |
| Osjetljivo | Higroskopna |
| Merck | 14,1667 |
| Konstanta proizvoda rastvorljivosti (Ksp) | pKsp: 8,28 |
| Granice izloženosti | ACGIH: TWA 2,5 mg/m3 NIOSH: IDLH 250 mg/m3; TWA 2,5 mg/m3 |
| Dielektrična konstanta | 2.5 (Ambient) |
| Stabilnost: | Stabilno. Kalcijum fluorid je inertan prema organskim hemikalijama i mnogim kiselinama, uključujući HF. Polako će se rastvoriti u azotnoj kiselini. |
| InChIKey | WUKWITHWXAAZEY-UHFFFAOYSA-L |
| Reference CAS baze podataka | 7789-75-5(referenca za CAS bazu podataka) |
| NIST Chemistry Reference | Kalcijum fluorid (7789-75-5) |
| EPA sistem registra supstanci | Kalcijum difluorid (7789-75-5) |
| Sigurnosne informacije |
| Kodovi opasnosti | Xi,Xn |
| Izjave o riziku | 36/37/38 |
| Izjave o sigurnosti | 26-37/39-36 |
| RIDADR | 3288 |
| WGK Njemačka | 1 |
| RTECS | EW1760000 |
| Napomena o opasnosti | Iritantno |
| TSCA | Da |
| HS kod | 28261900 |
| Podaci o opasnim supstancama | 7789-75-5(Podaci o opasnim supstancama) |
| Toksičnost | LD50 ip kod miševa: 2638,27 mg/kg (Stratmann) |
| MSDS informacije |
| Provajder | Jezik |
|---|---|
| Kalcijum fluorid | engleski |
| SigmaAldrich | engleski |
| ACROS | engleski |
| ALFA | engleski |
| Upotreba i sinteza kalcijum fluorida |
| Hemijska svojstva | Kalcijum fluorid je glavni sastojak fluorita ili fluorita, hemijska formula je CaF2, bezbojni je kubni kristal ili beli prah. Relativna gustina je 3,18, tačka topljenja je 1423 stepena, tačka ključanja je oko 2500 stepeni. Rastvorljivost u vodi je minimalna, 100g vode može rastvoriti samo 0,0016g na 18 stepeni, nerastvorljiv je u acetonu, ali rastvorljiv u hlorovodoničkoj kiselini, fluorovodičnoj kiselini, sumpornoj kiselini, azotnoj kiselini i rastvoru soli amonijuma i ne može da reaguje sa razblaženim kiselina, ali može reagovati sa vrućom koncentrovanom sumpornom kiselinom i stvoriti fluorovodoničnu kiselinu, može formirati kompleks kada se rastvori u rastvoru soli aluminijuma i gvožđa (Fe3 +). Prirodni kalcijum fluorid je mineralni fluorit ili fluorit, često pokazuje sivu, žutu, zelenu, ljubičastu i druge boje, ponekad je bezbojan, proziran, sjajno staklo, krhak, a relativna gustoća je 3,01~3,25, ima značajan fenomen fluorescencije. Može se koristiti kao izvor fluora i materijala za izradu sistema fluorovodične kiseline, fluorida; a može se koristiti iu smislu proizvodnje stakla, emajla, glazure. Fluorit se uglavnom koristi kao fluks u metalurgiji, vrlo čisti fluorit se može koristiti za izradu specijalnih sočiva. Voda kada sadrži (1~1,5) × 10-6 kalcijum fluorid može spriječiti probleme sa zubima. Osim toga, može se koristiti u topljenju željeza i čelika, proizvodnji kemikalija, stakla, keramike. Čisti proizvod se može koristiti za katalizator dehidracije, dehidrogenacije. Učinkom rastvorljivih kalcijumovih soli (kalcijum karbonat ili kalcijum hidroksid) i natrijum fluorida ili fluorovodonične kiseline mogu se dobiti amonijum fluorid, kalcijum fluorid. |
| kristalna struktura | Kalcijum fluorid je jonski kristal sa anionima fluora u jednostavnom kubičnom nizu i kalcijumovim kationima na polovini kubnih mesta strukture. Kalcijumovi joni se takođe mogu smatrati da su na "proširenoj" fcc rešetki sa jonima fluora koji uzrokuju da njihovo razdvajanje rešetke bude 0.39 nm. Ovaj prikaz je prikazan na donjem dijagramu. Jedinična ćelija ima 4 Ca2+joni i 8 F1-joni.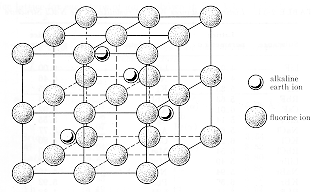 Materijal je transparentan u vidljivom spektralnom području i pokazuje elektronsku optičku adsorpciju u ultraljubičastom i rešetkastu optičku apsorpciju u infracrvenom. |
| Koristi |
Industrija
Aplikacija
Uloga/korist
Hemijska proizvodnja
Proizvodnja fluorovodonične kiseline i fluorida
Sirovi materijal/izvor fluorida
Proizvodnja finih hemikalija fluora i sintetičkog kriolita
Sirovi materijal/izvor fluorida
Arhitektonski materijal
Proizvodnja stakla
Sredstvo za fluksiranje/promoviše topljenje sirovina
Proizvodnja cementa
Sredstvo za mineralizaciju
Proizvodnja keramičke glazure
Fluksovi i pomoćna sredstva za bojenje
metalurgija
Topljenje željeza i čelika, proizvodnja ferolegura itd.
Sredstvo za fluksiranje/smanjenje tačke topljenja vatrostalnih supstanci
Lijek
Liječenje, kontrola, prevencija i poboljšanje alergijskih reakcija
Promoviranje stvaranja novih kostiju
Termovizijski sistemi, spektroskopija, teleskopi i ekscimer laseri
Proizvodnja optičkih komponenti, kao što su prozori i sočiva
Sirovi materijal/široki raspon frekvencija prijenosa svjetlosti; nizak indeks loma; visoka termo stabilnost
Drugi
Proizvodnja sredstava za zavarivanje
Važne komponente u premazima šipki za zavarivanje i prahu za zavarivanje
Dehidracija i reakcija dehidrogenacije
Katalizator/ubrzavanje procesa reakcije
Proizvodnja kočionih obloga
Aditiv/pomaže u smanjenju abrazije uzrokovane visokom toplinom i trenjem
|
| Način proizvodnje | Ležišta fluorita koja su pronađena u Kini, uglavnom se koriste u rudniku metodom podzemne eksploatacije, ili plitkim otvorenim kopom, i podzemnim dubokim kopanjem, za rudno tijelo najviše nagnute vene, proširenje je također veliko. Metoda rudarenja se zasniva na metodi skupljanja u plitkoj rupi. Proces rudarenja vidi "fosfat". Metode obogaćivanja općenito imaju dvije vrste, jedna je sirova ruda koja može postati kvalificirani koncentrat rude rukovanjem selekcijom, druga je ručno odabrana mršava ruda i jalovina. |
| Opis | Kalcijum fluorid je bezbojna kristalna ili bijela, praškasta supstanca. Molekulska težina{{0}}.08;Specifična težina (H2O:1)=3.18 na 20 stepeni; Tačka ključanja=2495 stepen ; Tačka smrzavanja/taljenja =1423 stepen . Identifikacija opasnosti (zasnovano na NFPA-704 M rejting sistemu): zdravlje 2, zapaljivost 0, reaktivnost 0. Praktično nerastvorljiv u vodi. |
| Hemijska svojstva | Kalcijum fluorid, CaF2, takođe poznat kao fluorit i feldspat, je bezbojna čvrsta supstanca sastavljena od kubnih kristala. Slabo je rastvorljiv u vodi, ali je lako rastvorljiv u rastvorima amonijumove soli. Kalcijum fluorid se koristi u sintezi fluorovodonične kiseline i u jetkanju stakla. Kalcijum fluorid nije higroskopan i relativno je inertan. Ima dovoljno visoku otpornost na termičke i mehaničke udare i lako se proizvodi u različite geometrije detektora. Kalcijum fluorid ima veoma nizak pritisak pare, što mu omogućava da se koristi u širokom spektru aplikacija u vakuumu. Nerastvorljiv je u vodi i većini organskih rastvarača, što omogućava da se radioaktivni uzorci u rastvoru stave u direktan kontakt sa kristalom. Kalcijum fluorid je prozirni materijal koji se koristi za detekciju -zraka do nekoliko stotina keV i za detekciju naelektrisanih čestica. Zbog niskog atomskog broja, fotofrakcija materijala je relativno mala što ograničava njegovu upotrebu u spektrometriji zraka pri višim energijama. Međutim, nizak atomski broj čini kalcijum fluorid idealnim materijalom za detekciju -čestica zbog male količine povratnog raspršenja. |
| Fizička svojstva | Bijeli kubični kristal ili prah; indeks prelamanja 1,434; gustina 3,18 g/cm3; tvrdoća 4 Mohs; topi se na 1.418 stepeni; isparava na 2.533 stepena; nerastvorljiv u vodi (16 mg/L na 20 stepeni); Ksp 3,9x10-11; slabo rastvorljiv u razblaženoj mineralnoj kiselini; rastvorljiv u koncentrisanim kiselinama (sa reakcijom). |
| Koristi | CaF2 koji se pojavljuje u prirodi je glavni izvor fluorovodonika, hemikalije koja se koristi za proizvodnju širokog spektra materijala. Fluorid se oslobađa iz minerala djelovanjem koncentrirane sumporne kiseline: CaF2 (čvrsto)+H2SO4 (tečnost)→CaSO4 (čvrsto)+2HF (gas) CaF2 se koristi kao optička komponenta zbog svoje hemijske stabilnosti u nepovoljnim uslovima. Kalcijum fluorid se obično koristi kao materijal za prozore i za infracrvene i za ultraljubičaste talasne dužine, pošto je providan u ovim regionima (oko 0.15 do 9 mm) i pokazuje izuzetno nizak indeks loma. Kalcijum fluorid je izvor kalcijuma nerastvorljiv u vodi za upotrebu u aplikacijama osetljivim na kiseonik, kao što je proizvodnja metala. U izuzetno niskim koncentracijama (ppm), spojevi fluora se koriste u zdravstvenim aplikacijama. Jedinjenja fluorida također imaju značajnu upotrebu u sintetičkoj organskoj hemiji. Takođe se obično koriste za legiranje metala i za optičko taloženje. Koristi se i kao fluks za topljenje i preradu u tečnost željeza, čelika i njihovih kompozita. Njegovo djelovanje je zasnovano na njegovoj sličnoj tački topljenja kao i željezo, na njegovoj sposobnosti da rastvara okside i na njegovoj sposobnosti da vlaže okside i metale. |
| Koristi | Fluorspar je glavni primarni izvor fluora i njegovih spojeva. U crnoj metalurgiji se koristi kao fluks za povećanje fluidnosti šljake. Industrija čelika je najveći potrošač; hemijska industrija, drugo i staklo i keramika, treće. Sintetički fluorit se koristi u optičkoj industriji (propušta uv zrake), a čisti kalcijum fluorid se koristi kao katalizator u dehidraciji i dehidrogenaciji. Koristi se za fluoriranje vode za piće. |
| Koristi | Kalcijum fluorid je komercijalno važan izvor jedinjenja fluorida kao i vodonik fluorida. Proziran je od ultraljubičastog do infracrvenog područja. Koristi se u spektroskopiji, termovizijskim sistemima i ekscimer laserima; također se koristi u proizvodnji optičkih komponenti uključujući prozore, prizme i sočiva. Osim toga, koristi se iu aluminijsko-metalurgiji, industriji proizvodnje kočnih obloga, te u caklini zuba. |
| Definicija | Čisti prirodni oblik kalcijum fluorida. |
| Metode proizvodnje | Komercijalni proizvod se dobija od prirodnog mineralnog fluora, koji je pročišćen i u prahu. Takođe, može se istaložiti mešanjem rastvora natrijum fluorida sa rastvorljivom soli kalcijuma: Ca(BR3)2+ 2NaF → CaF2+ NaNO3 Alternativno, može se dobiti tretiranjem kalcijum karbonata sa fluorovodoničnom kiselinom:CaCO3+ 2HF → CaF2+ CO2 + H2O. |
| Definicija | Mineralni oblik kalcijum fluorida (CaF2), koristi se u izradi nekih cementa i vrsta stakla. |
| Opšti opis | Sivi prah ili granule bez mirisa. Tone u vodi. |
| Profil reaktivnosti | Kalcijum fluorid ima slabu oksidacionu ili redukcionu moć. Redoks reakcije se ipak mogu javiti. Većina jedinjenja u ovoj klasi je slabo rastvorljiva ili nerastvorljiva u vodi. Ako su rastvorljivi u vodi, tada rastvori obično nisu ni jako kiseli ni jako bazični. Ova jedinjenja ne reaguju na vodu. |
| Hazard | Iritant. |
| Opasnost po zdravlje | Mala akutna toksičnost |
| Zapaljivost i eksplozivnost | Nije zapaljivo |
| Industrijska upotreba | Takođe se naziva fluorit, fluorit je kristalni ili masivni granulirani mineral sastava CaF2, koji se koristi kao fluks u proizvodnji čelika, za proizvodnju fluorovodonične kiseline, u opalescentnom staklu, u keramičkim emajlima, za uvijanje umjetnog kriolita, kao vezivo za staklaste abrazivne točkove i u proizvodnji bijelog cementa. To je bolji fluks za čelik od krečnjaka, stvara tečnu šljaku i oslobađa željezo od sumpora i fosfora. Acid Spar je vrsta koja se koristi u proizvodnji fluorovodonične kiseline. Takođe se koristi za proizvodnju rashladnih sredstava, plastike i hemikalija, kao i za redukciju aluminijuma. Optički fluorit je najvišeg kvaliteta, ali nije uobičajen. Kristali fluorida za optička sočiva uzgajaju se umjetno iz kiselog fluorita. Čisti kalcijum fluorid, Ca2F6, je bezbojni kristalni prah koji se koristi za jetkanje stakla, emajla i za smanjenje trenja u ležajevima mašina. Također se koristi za keramičke dijelove otporne na fluorovodoničnu kiselinu i većinu drugih kiselina. Kalcijum fluorit ima silicijum u molekulu i kristalni je prah koji se koristi za emajl. Prozirni rombični kristali fluorida koji se koriste za transformaciju električne energije u svjetlo su olovni fluorid, PbF2. |
| Sigurnosni profil | Umjereno toksičan intraperitonealnim putem. Blago toksično pri gutanju. Eksperimentalni teratogen. Drugi eksperimentalni reproduktivni efekti. Podaci o mutaciji prijavljeni. Vidi također FLUORIDI i JEDINJENJA KALCIJUMA. Kada se zagrije do raspadanja, emituje otrovne pare F-. |
| Potencijalna izloženost | Kalcijum fluorid se koristi za proizvodnju fluorovodonične kiseline; kao fluks u proizvodnji čelika; u topionici; elektrolučno zavarivanje, izrada stakla i keramike; i za fluorisanje vode za piće. |
| Prva pomoć | Ako ova hemikalija dospije u oči, odmah uklonite kontaktna sočiva i odmah ih isperite najmanje 15 minuta, povremeno podižući gornje i donje kapke. Odmah potražite medicinsku pomoć. Ako ova kemikalija dođe u kontakt s kožom, skinite kontaminiranu odjeću i odmah operite sapunom i vodom. Odmah potražite medicinsku pomoć. Ako je ova hemikalija udahnuta, uklonite iz izlaganja, počnite s disanjem za spašavanje (koristeći univerzalne mjere opreza, uključujući masku za oživljavanje) ako je disanje prestalo i CPR ako je srčana aktivnost prestala. Odmah prebacite u medicinsku ustanovu. Kada se ova hemikalija proguta, potražite medicinsku pomoć. Ovlašteni bolničar može razmotriti primjenu gela aluminijum hidroksida, ako je pri svijesti. |
| skladištenje | Šifra boje-zelena: Može se koristiti opšte skladištenje. Čuvati u dobro zatvorenim posudama na hladnom, dobro provetrenom prostoru dalje od kiselina i hemijski aktivnih metala (kao što su kalijum, natrijum, magnezijum i cink) jer će se proizvoditi korozivni fluorovodonik. |
| Dostava | Kalcijum fluorid nije posebno obuhvaćen DOT-om u svojim standardima pakovanja orijentisanih na performanse. |
| Inkompatibilnosti | Prašina može stvoriti eksplozivnu smjesu sa zrakom. Reaguje sa vodom, vlažnim vazduhom i parom, oslobađajući zapaljivi vodonik; i može se samozapaliti u vazduhu. Snažan redukcijski agens; nekompatibilan sa oksidantima (hlorati, nitrati, peroksidi, permanganati, perhlorati, hlor, brom, fluor, itd.); kontakt može izazvati požar ili eksploziju. Čuvati dalje od alkalnih materijala, jakih baza, jakih kiselina, oksokiselina, epoksida. Nekompatibilno sa metalnim halogenatima, srebrnim fluoridom i tetrahidrofuranom |
| Proizvodi i sirovine za pripremu kalcijum fluorida |
| Sirovine | Hydrogen fluoride-->Calcium hydroxide-->CARBON MONOXIDE-->Quartz-->Calcium acetate-->kalcijum magnezijum fosfat (CMP) |
| Proizvodi za pripremu | Hydrogen fluoride-->Boron trifluoride diethyl etherate-->Potassium Phosphate Monobasic-->Hexafluorosilicic acid-->Calcium cyanamide-->Sodium fluoride-->Trisodium hexafluoroaluminate-->Aluminum fluoride-->bastnasite-->Carbon tetrafluoride-->cryolite-->ZINC SILICOFLUORIDE-->MAGNEZIJ HEXAFLUOROACETILACETONAT DIHIDRAT |
Popularni tagovi: kalcijum fluorid, Kina proizvođači kalcijum fluorida, dobavljači, tvornica
Par: Cink Fluorid
Sljedeći: Stroncijum fluorid
Moglo bi vam se i svidjeti
Pošaljite upit


